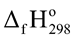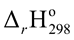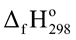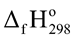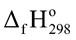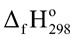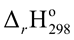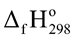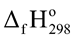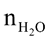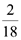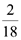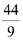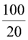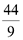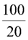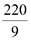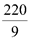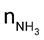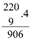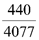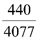Câu 5: Trong quá trình sản xuất nitric acid (HNO3), người ta sử dụng phản ứng oxi hóa ammonia (NH3) bằng oxygen (O2) theo phương trình sau:
4NH3(g) + 5O2(g) 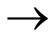 4NO(g) + 6H2O(g) (1)
4NO(g) + 6H2O(g) (1)
Phản ứng (1) là phản ứng tỏa nhiệt. Để tận dụng nhiệt lượng tỏa ra từ phản ứng (1), người ta dùng nó để đun nóng nước theo phương trình sau:
H2O (l) 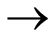 H2O (g) (2)
H2O (g) (2)
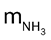
Xét các phản ứng ở điều kiện chuẩn và hiệu suất chuyển hóa của ammonia là 100%. Tính khối lượng ammonia (theo tấn, làm tròn kết quả đến hàng phần trăm) cần thiết để đun sôi 2,00 tấn nước. Biết 20% lượng nhiệt tỏa ra từ phản ứng (1) được sử dụng để đun sôi nước và các giá trị nhiệt tạo thành (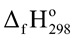 ) của các chất ở điều kiện chuẩn được cho trong bảng sau:
) của các chất ở điều kiện chuẩn được cho trong bảng sau:
|
Chất |
NH3(g) |
NO(g) |
H2O(g) |
H2O(l) |
|
|
-45,9 |
90,3 |
-241,8 |
-285,8 |
Câu 6: Một trong các phương pháp dùng để loại bỏ sắt trong nguồn nước nhiễm sắt là sử dụng lượng vôi tôi vừa đủ để tăng pH của nước nhằm kết tủa ion sắt khi có mặt oxi, theo sơ đồ phản ứng:
(1) Fe3+ + OH- → Fe(OH)3
(2) Fe2+ + OH- + O2 + H2O → Fe(OH)3
Một mẫu nước có hàm lượng sắt cao gấp 42 lần so với ngưỡng cho phép quy định là 0,30 mg/l (theo QCVN01-1:2018/BYT). Giả thiết sắt trong mẫu nước trên chỉ tồn tại ở hai dạng là Fe3+ và Fe2+ với tỉ lệ mol Fe3+ : Fe2+ = 1 : 3. Cần tối thiểu m gam Ca(OH)2 để kết tủa hoàn toàn lượng sắt trong 8 m³ mẫu nước trên. Giá trị của m là bao nhiêu? (làm tròn kết quả đến phần nguyên).
Đề thi thử TN THPT 2025 - Cấu trúc mới - Môn Hóa Học - Đề 29 - File word có lời giải