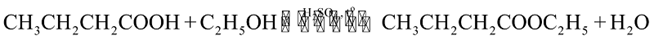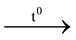|
ĐỀ THI THỬ CHUẨN CẤU TRÚC MINH HỌA ĐỀ 28 (Đề thi có 04 trang) |
KỲ THI TỐT NGHIỆP THPT NĂM 2025 MÔN: HÓA HỌC Thời gian làm bài 50 phút; không kể thời gian phát đề |
- Tải file word kèm ma trận và lời giải chi tiết ( 20k/Đề ) - LH Zalo 0915347068
Họ, tên thí sinh: .....................................................................
Số báo danh: ..........................................................................
* Cho biết nguyên tử khối của các nguyên tố: H = 1; He = 4; C = 12; N = 14; O = 16; Na = 23; Mg = 24; Al = 27; S = 32; Cl = 35,5; K = 39; Ca = 40; Cr = 52; Mn = 55; Fe = 56; Cu = 64; Zn = 65; Br = 80; Ag = 108; Ba = 137.
* Các thể tích khí đều đo ở điều kiện chuẩn, giả thiết các khí sinh ra không tan trong nước.
PHẦN I. Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn 1 phương án.
Câu 1: Trong hiện tượng ăn mòn kim loại xảy ra quá trình nào sau đây?
A. Quá trình khử kim loại. B. Sự mài mòn kim loại.
C. Quá trình oxi hoá kim loại. D. Quá trình điện phân.
A. calcium chloride. B. calcium carbonate.
C. calcium oxide. D. calcium hydrogencarbonate.
A. chất độn. B. chất tạo màu. C. chất hoá dẻo. D. polymer.
Câu 4: Hình ảnh sau đây minh họa tính chất vật lí nào của kim loại?
A. Tính dẫn điện. B. Tính dẫn nhiệt. C. Tính dẻo. D. Tính ánh kim.
Câu 5: Ở trạng thái cơ bản, nguyên tố nào sau đây có 2 electron ở lớp ngoài cùng ?
A. O (Z = 8). B. Ca (Z = 20). C. K (Z = 19). D. N (Z = 7).
A. CaSO3 + 2HCl → CaCl2 + SO2 + H2O.
B. Ca(HCO3)2 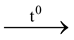 CaCO3 + CO2 + H2O.
CaCO3 + CO2 + H2O.
C. CaCO3 + 2HCl → CaCl2 + CO2 + H2O.
D. Ca(HCO3)2 + 2HCl → CaCl2 + 2CO2 + 2H2O.
Câu 7: Tiêu lệnh chữa cháy do cục cảnh sát phòng cháy, chữa cháy ban hành bao gồm các bước:
(a) Dùng bình chữa cháy cát và nước để dập tắt.
(b) Điện thoại số 114 đội chữa cháy chuyên nghiệp.
(c) Khi xảy ra cháy báo động gấp.
(d) Cúp cầu dao điện nơi xảy ra cháy.
Thứ tự đúng của các bước trên là
A. (c), (d), (a), (b). B. (d), (b), (a), (c). C. (d), (c), (a), (b). D. (c), (d), (b), (a).
A. Calcium, magnesium. B. Sodium, potassium.
C. Chloride, sulfate. D. Nitrate, phosphate.
A. acetone. B. glycine. C. ethyl acetate. D. acetic acid.
Câu 10: Chất nào sau đây là thành phần chính của xà phòng ?
A. C17H35COONa. B. CH3COONa. C. CH3[CH2]3COONa. D. CH2=CHCOONa.
Câu 11: Số đồng phân cấu tạo là amine bậc một ứng với công thức phân tử C3H9N là
Câu 12: Công thức cấu tạo dạng mạch hở của glucose là
A. [C6H7O2(OH)3]n. B. CH2OH(CHOH)4CHO.
C. CH2OH(CHOH)4CH2OH. D. CH2OH(CHOH)3COCH2OH.
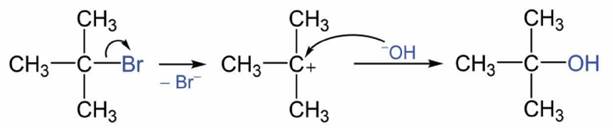
Câu 13: Cho tert-butyl bromide tác dụng với dung dịch NaOH như sau:
(CH3)3CBr + NaOH 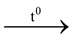 (CH3)3C-OH + NaBr (I)
(CH3)3C-OH + NaBr (I)
A. Phản ứng (I) là phản ứng cộng.
B. Trong phân tử tert-butyl bromide có 12 liên kết σ.
C. Giai đoạn 1 của cơ chế phản ứng có sự phân cắt liên kết π.
D. Trong giai đoạn 1 của cơ chế phản ứng có sự hình thành carbocation.
Câu 14: Ester X được tạo bởi ethyl alcohol và formic acid. Công thức của X là
A. CH3COOCH3. B. CH3COOC2H5. C. HCOOC2H5. D. HCOOCH3.
Câu 15: Phát biểu nào sau đây không đúng?
A. Protein tác dụng với Cu(OH)2 trong môi trường kiềm tạo dung dịch màu xanh lam.
B. Protein bị đông tụ khi đun nóng ở nhiệt độ cao.
C. Thuỷ phân hoàn toàn protein thu được các phân tử α-amino acid.
D. Protein tác dụng với nitric acid đặc tạo kết tủa vàng.
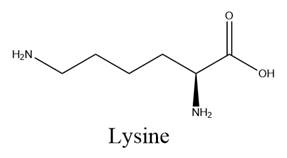
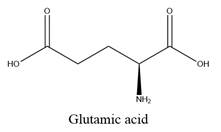
(a) Khi pH = 1 thì glutamic acid và lysine đều di chuyển về cực âm (cathode).
(c) Khi pH = 6 thì glutamic acid di chuyển về phía cực âm còn lysine di chuyển về phía cực dương.
Có bao nhiêu kết luận là đúng?
A. Al3+. B. Ag+. C. Fe2+. D. Cu2+.
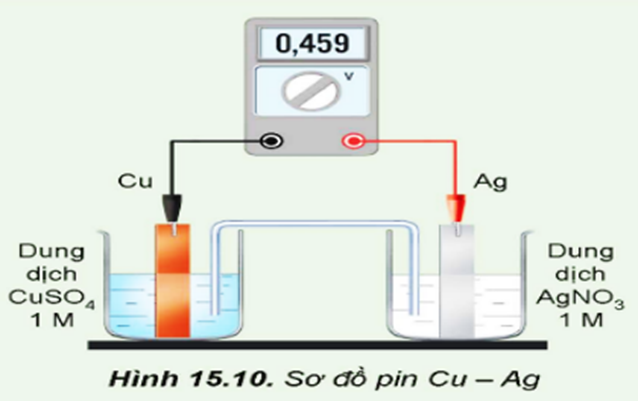
Câu 18: Một pin Galvani được thiết lập ở điều kiện chuẩn theo sơ đồ sau:
Cho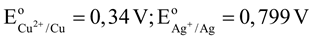 . Phát biểu nào sau đây sai?
. Phát biểu nào sau đây sai?
A. Thanh Cu là nguồn cung cấp electron nên đóng vai trò là anode.
B. Thanh Ag là nơi nhận electron nên đóng vai trò là cathode.
C. Phương trình hoá học của phản ứng xảy ra trong pin: 2Ag + Cu2+ → 2Ag+ + Cu.
D. Sức điện động chuẩn của pin là 0,459 (V).
PHẦN II. Câu hỏi trắc nghiệm đúng sai. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu thí sinh chọn đúng hoặc sai.
- Cân để xác định khối lượng ban đầu của chìa khóa (35,12 gam) và đồng xu (5,30 gam).
- Điện phân ở hiệu điện thế phù hợp.
a) Ở cực dương xảy ra quá trình oxi hóa.